TYT-Kimya 18. Kimyasal Hesaplamalar-1
Madde Miktarının Verildiği Problemler
Bir tepkimede harcanan ya da elde edilen maddelerden herhangi birinin miktarı bilinirse tepkimedeki diğer maddelerin harcanan ya da elde edilen miktarları ayrı ayrı belirlenebilir.
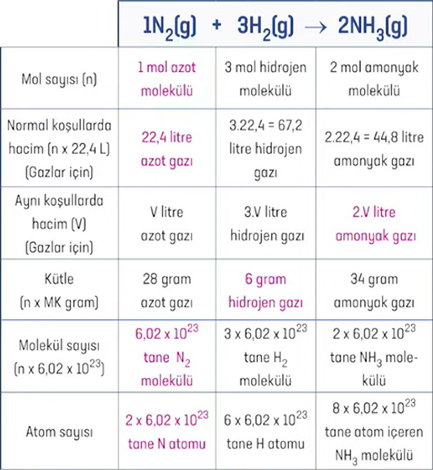
Bir tepkimenin denklemindeki maddelerin önünde bulunan katsayılar mol olarak ifade edilir ve denklemdeki madde miktarları bu katsayılara göre belirlenir.
Denklemdeki miktarlar ile soruda verilen ve istenen miktarlar arasında bir doğru orantı kurularak hesaplamalar yapılır.
- Artansız tepkime: tepkimeye giren maddelerin tamamının tükendiği tepkimelerdir.
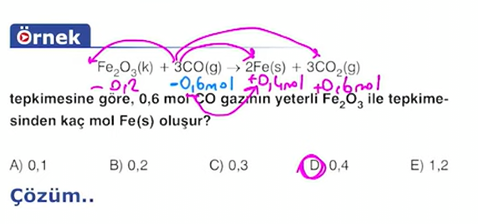
- Tam verimli tepkime: tepkimeye giren maddelerden en az birinin tükendiği tepkimelerdir. Reaktiflerden birinin "yeter miktarda" olduğu belirtildiğinde ya da ürünlerden birinden "en fazla" oluşan miktarı belirtildiğinde tepkime tam verimli demektir.

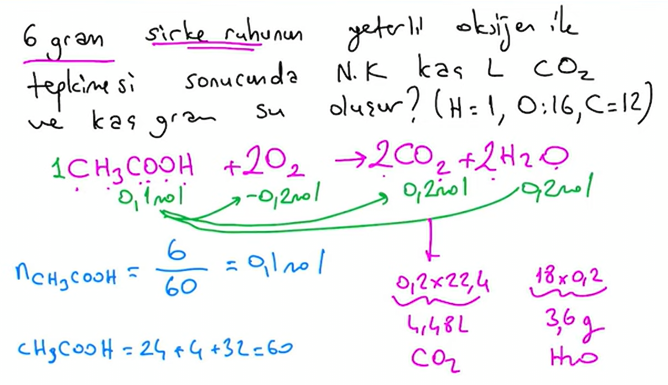
Gazların hacmini mol ile bulmak için, kapladığı hacmi, aynı koşullarda bir mol gazın kapladığı hacme böl.

Aynı Anda Oluşan Tepkimeler
- Aynı anda birden çok maddenin tepkimeye girdiği soru türleridir.
- Bu tür sorularda her maddenin tepkimesi ayrı ayrı yazılarak işlem yapılır.


Bir metal asit ile tepkimeye girdiğinde çıkan hidrojenin katsayısı metalin değerliğinin yarısı kadardır.

Kademeli tepkime sorularında üstte elde edilen madde miktarı ne ise, aşağıya da bu miktar aynen yazılır!

