Çözünürlük-1
Çözeltilerin Sınıflandırılması
Çözeltiler; çözünen ve çözücüden oluşan homojen karışımlardır.
Gene olarak miktarı az olana çözünen, çok olana çözücü denir. Ancak gaz karışımlarında genelde bu şekilde bir ayrım yoktur.
Çözeltiler çözünürlük temelinde aşağıdaki gibi sınıflandırılır.
- Seyreltik Çözelti: Çözünen/çözücü oranı bir başka çözeltiye göre düşük olan çözeltilerdir.
- Derişik Çözelti: Çözücü/çözünen oranı bir başka çözeltiye göre yüksek olan çözeltilerdir.
Derişik ve seyreltik terimleri karşılaştırmalı ve göreceli kavramlardır.
- Doymamış Çözelti: Belirli sıcaklık ve basınç koşullarında belirli miktar çözücüde çözebileceğinden daha az çözünen içeren çözeltilere doymamış çözelti denir.
- Doymuş Çözelti: Belirli sıcaklık ve basınç koşullarında belirli miktar çözücüde çözebileceği en fazla miktarda çözüneni çözmüş olan çözeltilere doymuş çözelti veya dipte katısıyla dengede çözelti denir.
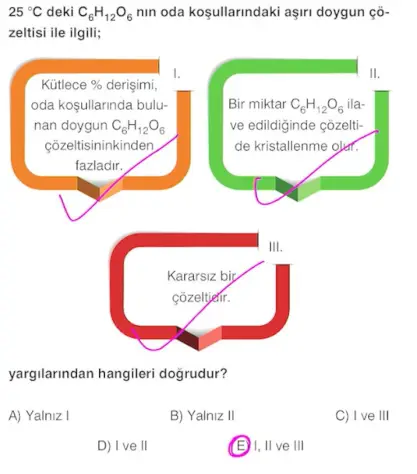
- Aşırı Doymuş Çözelti: Belirli sıcaklıkta doymuş çözelti oluşturmak için gerekli olandan daha fazla çözünen içeren çözeltilere denir. Aşırı doygun çözelti kararsızdır. Çözeltinin çalkalanması veya aşı kristali (aynı maddeden biraz daha) atılmasıyla doygunluk sınırını aşan miktar kristallenip dibe çöker ve doygun çözelti oluşur.
Farklı maddelerin doymuş/doymamış çözeltilerinde ve doymuş/doymamış karşılaştırması yapılamaz. Çünkü bir maddenin suda 1 gramının çözünmesiyle su doymuş hale gelebiliyorken başka bir madde 100 gram çözünse de doymamış olabilir.
Aşırı doymuş bir çözelti elde edebilmek için sıcaklığı değiştirmek gerekir.
Çözünürlük
Belirli sıcaklık ve basınçta 100 gram çözücüde çözünen madde miktarına çözünürlük denir.
Çözünürlük birimi genellikle g/100g su olarak kullanılır.
\[\text{Çözünürlük} = \frac{m_{\text{çözünen}}(g)}{\text{100g çözücü}} \]
Çözeltilerin doymuş, doymamış, aşırı doymuş olduğuna çözünürlüklerine bakılarak karar verilir.
Örneğin \(25\degree C\) da \(KNO_3\) tuzunun saf sudaki çözünürlüğü 38 gramdır. Buna göre:
- \(25\degree C\) da 100 gram suda en fazla 38 gram \(KNO_3\) çözülebilir.
- \(25\degree C\) da 100 gram suda 38 gram \(KNO_3\) çözülürse doymuş, daha az çözülürse doymamış çözelti elde edilir. Sıcaklık değiştirilerek kontrollü bir şekilde daha fazla \(KNO_3\) çözülebilirse aşırı doymuş çözelti elde edilir.
Çözünürlüğe Etki Eden Faktörler
Çözücü Türü
Saf maddelerin çözünürlüğü çözücü sıvının türüne göre değişir.
Örneğin apolar bir madde olan \(CS_2\), polar bir madde olan saf suda az çözünürken, apolar bir madde olan \(CCl_4\) te daha fazla çözünür.
Sıcaklık
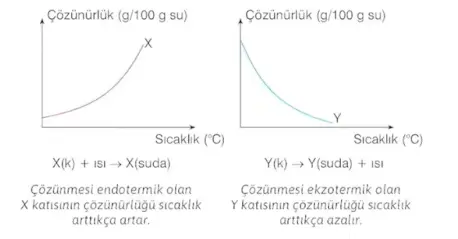
Genellikle katı ve sıvıların çözünürlüğü sıcaklık arttıkça artar. Bazı katıların ise çözünürlüğü sıcaklık arttıkça azalır.
- Suda çözünmesi endotermik olan (ısı alan) maddelerin çöznürlüğü sıcaklık arttıkça artarken
- Suda çözünmesi ekzotermik olan (ısı veren) maddelerin çözünürlüğü sıcaklık arttıkça azalır.
Gazların tamamının suda çözünmesi ekzotermiktir. Bu nedenle tüm gazlar için sıcaklık arttıkça çözünürlük azalır.
- Katıların çözünmesi genellikle endotermiktir.
Sıcak havalarda göllerde balık ölümleri gerçekleşebilir. Bunun sebebi sıcaklık arttıkça suda çözünebilen maksimum oksijenin azalmasıdır. Sudaki oksijen azaldığında da balıklar gluk gluk olup vefat eder.
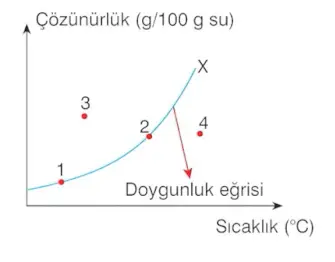
Saf X katısına ait şekil 10'daki çözünürlük-sıcaklık grafiğinden numaralandırılmış duruma ilgili;
- 1 ve 2 durumlarında X çözeltisi doygundur. Ancak X'in 2 durumdaki çözünürlüğü 1 durumundakinden daha yüksektir.
- 3 durumundaki çözelti aşırı doymuştur. Bu çözeltiyi doymuş hale getirmek için; fazla madde dibe çöktürülebilir, sıcaklık arttırılabilir veya daha fazla çözücü eklenebilir.
- 4 durumundaki çözelti doymamış bir çözeltidir. Bu çözeltiyi doymuş hale getirmek için; fazla su buharlaştırılabilir, sıcaklık düşürülebilir veya daha fazla X maddesi eklenebilir.
Basınç
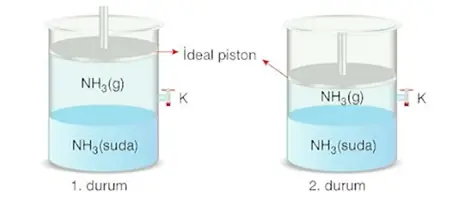
Katı ve sıvıların sıvılardaki çözünürlüğüne basıncın etkisi yoktur. Gazların sıvılardaki çözünürlüğü ise basınç arttıkça artar.
Şekil 20'deki durumlardan birincisinde çözeltisiyle denge halinde bulunan amonyak gazı vardır. Piston sabit sıcaklıkta biraz aşağı itildiğinde ikinci durum elde edilmiştir. İkinci durumda \(NH_3(g)\) basıncı arttığından \(NH_3(g)\) gazının sudaki çözünürlüğü birinci durumdakinden daha fazladır.
Gazların çözünürlüğüne basıncın etkisine ait günlük hayattan gazoz vb. gazlı içeceklerin kapağı açıldığında oluşan şiddetli gaz çıkışı ve dalgıçların vurgun olayı örnek olarak verilebilir
Amonyak bazdır, bilmeyen kazdır.
Ortak İyon
Ortak iyon çözünürlüğü azaltan bir faktördür.
Çözünürlüğe ortak iyonun etkisi "Kimyasal Tepkimelerde Denge" ünitesinde, çözünme-çökelme tepkimeleri bölümünde işlenecektir.
Questions



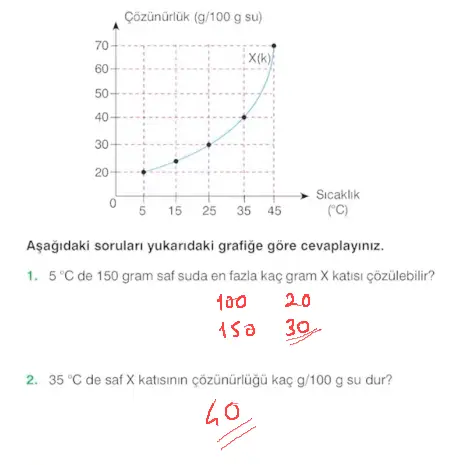

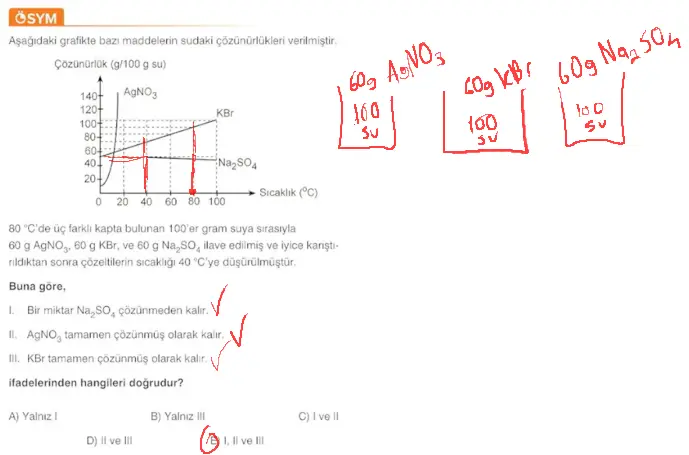

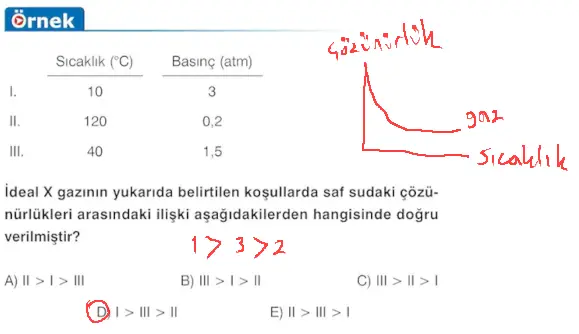
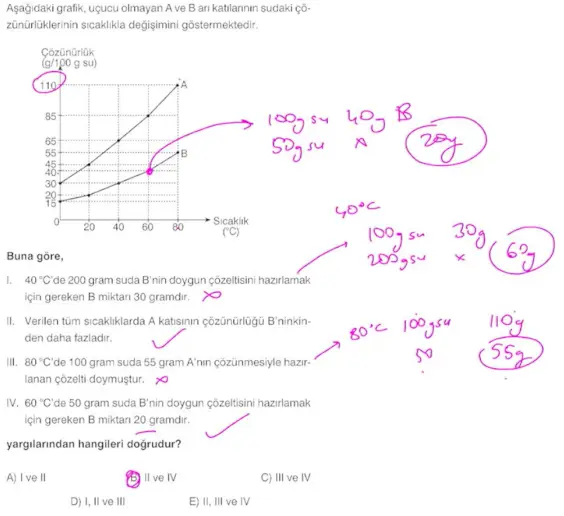




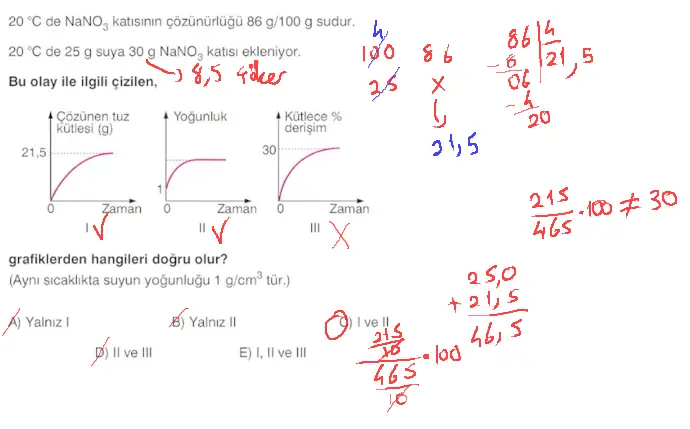


- Molar derişim artarsa çözünen madde miktarı da artar.