Hız Bağıntısı Yazma
Ortalama Reaksiyon Hızları
Herhangi bir tepkimenin başlangıç ve bitiş anına kadar harcanan ya da elde edilen madde derişimleri ve tepkimenin toplam süresine göre hesaplanan hıza reaksiyonun ortalama hızı denir.
\[\text{Ortalama Hız}=\frac{\text{Derişim Değişimi}}{\text{Geçen Zaman}} \]
Tepkimenin herhangi bir andaki hızı ile ortalama hız birbirinden farklıdır. Ancak genel olarak ortalama hız yerine reaksiyon hızı ifadesi kullanılır.
Tepkimelerde Hız Bağıntıları
Tek Basamaklı Tepkimeler ve Hız Bağıntısı
Tek basamaklı tepkimelerin hız bağıntısı yazılırken, hız sabiti (k) ile reaktif(girenlerin) derişimleri çarpılır. Reaktif(girenlerin) derişimlerinin katsayıları derişime üs olarak yazılır. Örneğin;
\[\ce{aX(g) + bY(g) -> Z(g) + cD(g)} \]
Tepkimesinde tepkimenin hız bağıntısı aşağıdaki gibidir.
\[\text{Hız}=k.[X]^a.[Y]^b \]
- Formüldeki k sabitine hız sabiti denir. Her tepkimenin kendine özgü bir hız sabiti vardır. Derişimler ve hız sabiti kullanılarak yazılan bağıntılardaki hız birimi, her zaman mol/L.s dir.
- Hız denklemindeki derişim terimlerinin üsleri yani a ve b nin toplamına tepkimenin mertebesi (derecesi) denir.
- Tepkime hız bağıntısına sadece sulu çözeltiler (suda,aq) ve gazlar (g) yazılır. Katı ve sıvılar yazılmaz. Çünkü katı ve sıvıların miktarı değiştirildiğinde derişimleri değişmez.
Katı ve sıvıların derişimi her zaman 1 kabul edilir. Bu sebeple denkleme yazılmasalar da olur.
Pratik olarak hız sabitinin (k) birimi; hız bağıntısında derişimlerin üslerinin toplamı x ise, aşağıdaki gibi bulunur.
- \(k=(L/mol)^{x-1}.(1/s)\)
Çok Basamaklı Tepkimeler ve Hız Bağıntısı
Birden fazla basamakta gerçekleşen tepkimelere mekanizmalı (basamaklı) tepkime denir.
- Mekanizmalı tepkimelerin hızları deneysel yollar ile belirlenir. Hız bağıntıları da toplam tepkimeye göre yazılmaz.
- Tepkimenin hızını, en yavaş basamak belirlediği için, hızın bağıntısı yavaş basamağın denklemine göre yazılır.
Örneğin, iki basamaklı aşağıdaki tepkimeyi incelersek;
- \(\ce{H2(g) + ICl(g) -> Hl(g) + HCl(g) (slow)}\)
- \(\ce{Hl(g) + ICl(g) -> I2(g) + HCl(g) (fast)}\)
- Net: \(\ce{H2(g) + 2ICl(g) -> I2(g) + 2HCl(g)}\)
Bu tepkimenin hız bağıntısı aşağıdaki gibidir.
\[\text{Hız}=k.[H_2]^1.[ICl]^1 \]
Yukarıda, 1. tepkimenin ürünlerinde açığa çıkıp 2. tepkimede kullanılan Hl maddesine de ara ürün adı verilir.
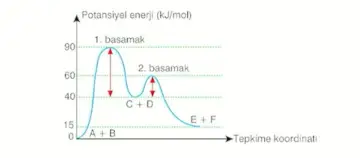
- İleri aktifleşme enerjisi ne kadar büyükse tepkime o kadar yavaştır.
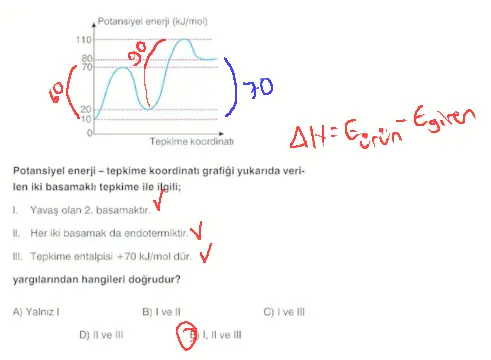
- Basamaklı tepkimelerin potansiyel enerji-tepkime koordinatı grafikleri çizilirken, her bir basamağın grafiği birbirini takip edecek şekilde çizim yapılır.
Şekil-3'teki grafiğe göre; net tepkime denklemi aşağıdaki gibidir.
- \(\ce{A(g) + B(g) -> C(g) + D(g) (slow)}\)
- \(\ce{C(g) + D(g) -> E(g) + F(g) (fast)}\)
Net: \(\ce{A(g) + B(g) -> E(g) + F(g)}\)
- Grafiğe göre, net tepkime endotermiktir.
- Net tepkimenin hız bağıntısı en yavaş olan 1. basamağın hız bağıntısı ile aynı olup \(k.[A].[B]\) şeklindedir.
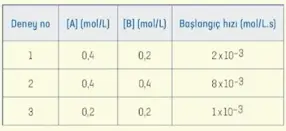
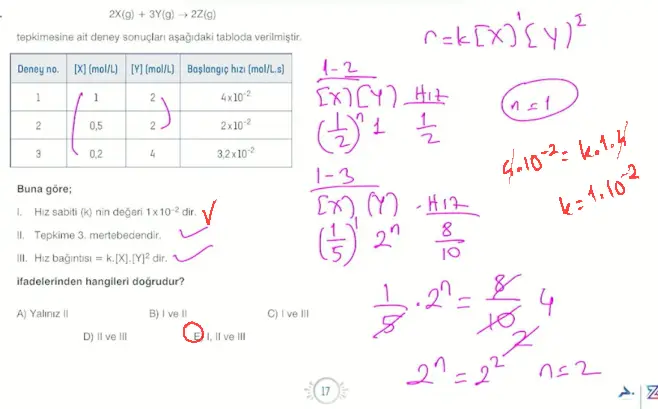
Çok basamaklı tepkimelerde derişim değişimli, deney sonuçlarından yararlanarak da tepkime hızı bulunabilir.
Hız bağıntısı bulunurken;
- Birinci ve ikinci deneyler karşılaştırıldığında; A'nın derişimi sabit iken B'nin derişimi iki katına çıkmıştır. Tepkime hızı ise 4 katına çıkmıştır. Bu nedenle tepkimenin hızı B'nin derişiminin karesi ile doğru orantılıdır.
- \(\text{Hız}\propto [B]^2\)
- Birinci ve üçüncü deneyler karşılaştırıldığında, B derişimi sabit iken A derişimi yarıya düşmüştür. Tepkime hızı ise yarıya düşmüştür. Bu nedenle tepkimenin hızı A'nın derişimi ile doğru orantılıdır.
- \(\text{Hız}\propto [A]\)
- Hız bağıntısı \(k.[A].[B]^2\) şeklinde yazılır.
Hız sabiti (k)'nın değeri ise
- Herhangi bir deneydeki veriler kullanılarak hız sabiti bulunabilir. Örneğin 2. deneydeki verileri kullanarak hesaplama yaptığımızda.
\[\text{Hız}=k.[A].[B]^2 \Longrightarrow 8.10^{-3} = k.(0,4).(0,4)^2 \Longrightarrow k=1/8 \]
Hız sabitinin birimi için;
- Hız denkleminde, değerler yerine her birinin birimini yaz ve k'yı yalnız bırak.
- Veya \(k=(L/mol)^{x-1}.(1/s)\) formülü ile de bulunabilir. (x: derişimlerin üslerinin toplamı)
Questions
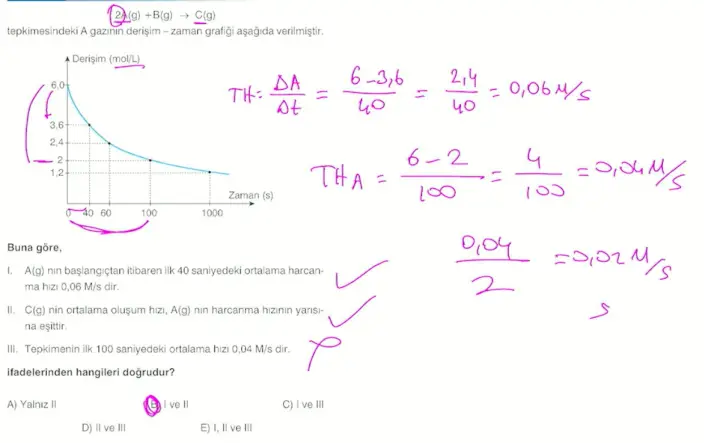
- Tepkimenin ortalama hızı, A'nın ortalama hızından farklıdır.
- Tepkime hızı katsayısı 1 olana göre düşünülür.
- Tepkimenin hızı, A'nın harcanma hızının 2'ye bölümüne eşittir.

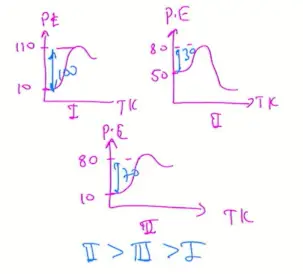
- Tepkime hızları karşılaştırıldığında 2 > 3 > 1 eşitliği bulunur.



- 2'den fazla girenin olduğu denklemlerde önce hızın değişmediği yere bakılarak çözüm kolaylaştırılabilir.


- Bunu tekrar çöz.
- H2'nin 200 saniyedeki molarite değişimi +0,012 ise, 2NH3'ün molarite değişimi -0,0,008 olur. Bu değişimi geçen süreye (200sn) bölerseka NH3'ün ortalama harcanma hızını buluruz.






- N2 sınırlayıcı bileşendir.

- Deneye göre hesapladığımız tepkime hızı ile denklemdeki tepkime hızı birbiriyle uyuşmadığı için tepkimenin birden fazla kademede gerçekleştiği yorumunu yapabiliriz.