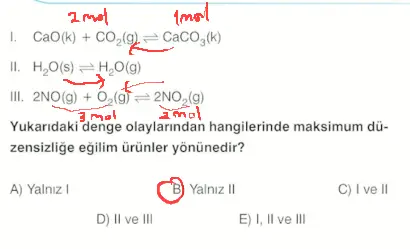
Kimyasal denge hesaplamaları
Kimyasal tepkimelerde hesaplardan yararlanılarak başlangıç miktarları ile harcanan ve oluşan miktarlar arasında ilişkiler kurularak denge anındaki miktar bulunabilir. Bu durumun tersinden de gidilebilen sorular olacaktır.
Tepkime denklemi ile denge sabiti arasındaki ilişki
Bir tepkimenin denge sabitinin sayısal değeri tepkime denklemi ve katsayıları ile doğrudan ilişkilidir. Tepkime denkleminin yönü ve katsayıları değiştirilirse denge sabiti de değişir.
Bir denge reaksiyonu ters çevrilirse, \(K_c\) denge sabiti \(1/K_c\) olur.
Bir tepkimenin katsayıları n ile çarpılırsa \(K_c\) denge sabiti \((K_c)^n\) olur.
- \(\ce{A(g) + B(g) <=> AB(g)},\quad K_c = a\)
- \(\ce{2A(g) + 2B(g) <=> 2AB(g)},\quad K_c = a^2\)
Herhangi bir tepkime diğer tepkimelerin toplamından oluşuyorsa, bu tepkimenin K_c değeri diğer tepkimelerin K_c değerlerinin çarpımına eşittir.
Herhangi bir tepkime diğer tepkimelerin toplamından oluşuyorsa, bu tepkimenin K_c değeri diğer tepkimelerin K_c değerlerinin çarpımına eşittir.
- \(\ce{AD + C <=> AC + D},\quad K_1=a\)
- \(\ce{CD + D <=> C + 2D},\quad K_1=a\)
- \(\ce{AD + CD <=> AC + 2D},\quad K_3=K_1.K_2=a.b\)
Questions



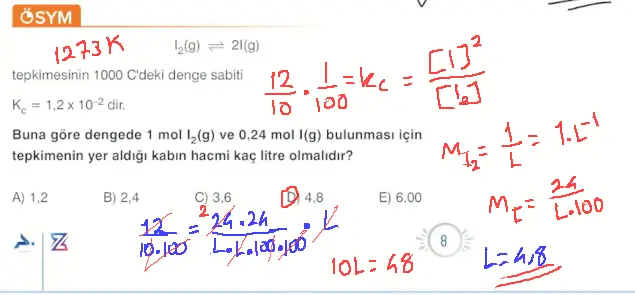


- Cevap maalesef şıklarda yok.
- Gazların yaptığı basınçlar mol sayıları ile doğru orantılıdır.