Kimyasal Dengeye Etki Eden Faktörler
Denklemi belirli olan bir tepkimenin denge sabitini etkileyen tek etken sıcaklıktır.
Denge halindeki bir sisteme dışarıdan yapılan bazı etkiler de denge sisteminin bozulmasına neden olabilir. Bu durumda denge sistemi tekrar denge durumuna ulaşmak üzere bir yöne doğru ilerler.
- Bir ya da birkaç maddenin derişiminin değiştirilmesi
- Sıcaklığın değiştirilmesi
- Denge sisteminin hacminin değiştirilmesi
Denge sisteminin denge durumunu değiştirebilen etkenlerdir.
Le Chatelier Ilkesi
Henry Le Chatelier (1850-1936) denge halindeki bir sisteme dışarıdan bir etkinin denge sistemini nasıl etkileyeceği konusunda araştırma yaparak kendi adıyla ifade edilen ilkeyi ortaya koyan bilim insanıdır.
Bu ilkeye göre "Denge halindeki bir sisteme dışarıdan bir etki yapılırsa (derişim, basınç, hacim ve sıcaklık değişikliği gibi) sistem daima bu etkiyi azaltıcı yönde davranış gösterir."
Derişim Değişimlerinin Dengeye Etkisi
Denge reaksiyonlarında yer alan maddelerin derişimlerinde meydana gelecek değişimler dengeyi etkiler.
Bir denge tepkimesinde,
- Girenlerin derişimi azaltılır veya ürünlerin derişimi artırılırsa denge girenler yönünde,
- Ürünlerin derişimi azaltılır veya girenlerin derişimi artırılırsa denge ürünler yönünde ilerler.
- Böylece tepkime tekrar dengeye ulaşır.
\[\ce{CH4(g) + 2H2S(g) <=> H2(g) + CS2(s)} \]
denge tepkimesinde \(t_1\) anında;
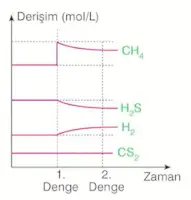
Sabit sıcaklık ve hacimde ortama \(CH_4\) gazı eklenirse:
- Denge ürünler yönünde kayar.
- \(H_2\) gazının derişimi artar, \(H_2S\) gazının derişimi azalır.
- \(CH_4\) gazının derişimi önce artar, sonra azalır. Ancak ilk duruma göre fazla olur.
- \(H_2S\) girenlerde olduğu ve denge ürünlere doğru kaydığı için azalır.
- \(H_2\) ürünlerde olduğu ve denge ürünlere doğru kaydığı için artar.
- \(CS_2\) maddesi sıvı olduğundan derişimi değişmez, ancak miktarı artar.
- Sonuç olarak denge sabiti \(K_c\) değişmez.
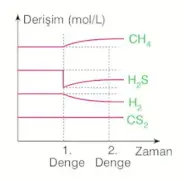
Sabit sıcaklık ve hacimde ortamdan \(H_2S\) gazı çekilirse:
- Denge girenler yönünde kayar.
- \(H_2\) derişimi azalır, \(CH_4\) derişimi artar.
- \(H_2S\) derişimi önce azalır, sonra artar. Ancak ilk duruma göre daha az olur.
- \(CH_4\) girenlerde olduğu ve denge girenler yönünde kaydığı için miktarı artar.
- \(CS_2\) maddesi sıvı olduğundan derişimi değişmez ancak miktarı azalır.
- Denge sabiti \(K_c\) değişmez.
Sabit Sıcaklık ve Hacimde Ortama \(CS_2\) Sıvısı Eklenirse:
- \(CS_2\) maddesi sıvı olduğundan ortama eklenmesi ya da ortamdan çekilmesi dengenin yönünü değiştirmez.
Denge Kesri (Qc)
Herhangi bir anda tepkimenin dengede olup olmadığını anlamak için bu andaki madde derişimleri denge bağıntısında yerine yazılarak bir değer elde edilir ve bu değer denge kesri \((Q_c)\) olarak adlandırılır. Denge kesrinin bir diğer adı yalancı denge sabitidir.
Aynı sıcaklıkta belirlenen \(Q_c\) değeri ile tepkimenin denge sabiti \(K_c\) değerleri karşılaştırılarak tepkimenin o anki duruöu ve dengeye ulaşana kadarki değişimleri hakkında yorum yapılır.
- \(Q_c = K_c\) ise tepkime dengededir.
- \(Q_c < K_c\) ise tepkime dengede değildir.
- Denge oluşana kadar, tepkime ürünler yönüne ilerler.
- Zamanla ürünlerin derişimi artar.
- Zamanla girenlerin derişimi azalır.
- Q_c > K_c ise tepkime dengede değildir.
- Denge oluşana kadar, tepkime girenler yönünde ilerler.
- Zamanla ürünlerin derişimi azalır.
- Zamanla girenlerin derişimi artar.
Sıcaklık Değişimlerinin Dengeye Etkisi
Sıcaklık değişimi tepkimenin endotermik veya ekzotermik oluşuna göre dengeyi etkiler.
- Sıcaklık değişimi denge sabitinin de değişmesine neden olur.
Endotermik Tepkimede Sıcaklığın Dengeye Etkisi
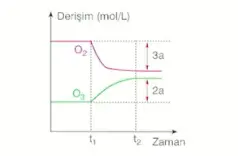
\[\ce{3O2(g) + 141kJ <=> 2O3(g)} \]
Sabit hacimde ortamın sıcaklığı artarsa ısı artar. Hem ileri hem de geri reaksiyon hızı artar. Ancak tepkime ısıyı azaltacak yönde hareket eder.
- Tepkime ürünler yönünde ilerler.
- Yeni denge oluşana kadar, \(O_2\) gazının derişimi azalır ve \(O_3\) gazının derişimi artar.
- Ürün derişimi artarken, giren derişimi azaldığı için denge sabiti \(K_c\) büyür.
- Tepkime madde katsayısı toplamının küçük olduğu yöne ilerlediği için toplam mol sayısı azalır.
Sabit hacimde ortamın sıcaklığı azaltılırsa tepkime ortamın ısısını artıracak yönde hareket eder. Yani tepkime girenler yönünde ilerler, \(K_c\) küçülür.
Ekzotermik Tepkimede Sıcaklığın Dengeye Etkisi
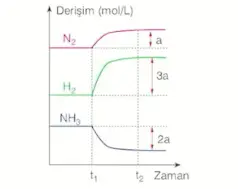
\[\ce{N2(g) + 3H2(h) <=> 2NH3(g) + 92kJ} \]
Sabit hacimde ortamın sıcaklığı yani ısısı artırıldığında, hem ileri hem de geri reaksiyon hızları artar. Ancak tepkime ısıyı azaltacak yönde hareket eder.
- Tepkime girenler yönünde ilerler.
- Yeni denge oluşana kadar \(N_2\) ve \(H_2\) gazlarının derişimleri artar ve \(NH_3\) gazının derişimi azalır.
- Ürün derişimi azalırken, giren derişimi arttığı için denge sabiti \(K_c\) küçülür.
- Tepkime madde katsayısı toplamının büyük olduğu yöne ilerlediği için toplam mol sayısı artar.
Ortamın sıcaklığı azaltılırsa tepkime ortamın ısısını artıracak yönde hareket eder. Yani tepkime ürünler yönünde ilerler, \(K_c\) büyür.
Denge sabiti yalnızca sıcaklıkla değişir. Denge, sıcaklıktan dolayı ürünler yönüne kaydığında denge sabiti büyür, girenler yönüne kaydığında denge sabiti küçülür.
Questions


- C şıkkı yanlıştır. \(t_1-t_2\) anında ileri ve geri yöndeki tepkime hızları eşittir. \(t_2-t_3\) anında ileri yöndeki geri yöndekinden büyüktür.
- Cevap E şıkkıdır.


- Üç mol Z gazı çekildiğinde Z gazı miktarı 6 mole düşer ve denge ürünler yönüne kayar. X ve Y, Z'ye dönüşmeye başlar.
- İkinci dengede X ve Y n'şer mol azalmış, Z, 2n mol artmıştır.


- Tepkime denkleminde ileri veya geri yönde gitmenin mol sayısını değiştirebileceği bir şey olmadığından, mol sayısı denge anında da sabit kalır.
