TYT-Kimya 13. Maddenin Halleri-3
- Previous: TYT-Kimya 12. Maddenin Halleri-2
- Next: TYT-Kimya 14. Doğa ve Kimya
Gazlar
Gazlar; sıcaklık, basınç, hacim ve madde miktarı gibi çeşitli değişkenlere bağlı olarak farklı fiziksel davranışlar gösterebilir.
- Tanecikleri arasındaki çekim kuvveti çok azdır ve birbirlerinden bağımsız hareket ederler.
- Belirli şekilleri ve hacimleri yoktur. Hacimleri bulundukları kabın hacmine eşittir.
- Düşük sıcaklık ve yüksek basınçta, sıkıştırılarak sıvı hale getirilebilirler.
- Sıcaklık etkisine göre genleşirler. Tüm gazların genleşme katsayıları aynıdır.
- Yoğunlukları katı ve sıvılara göre küçüktür.
- Gaz tanecikleri çok hızlı hareket eder ve maddenin en düzensiz halidir.
- Gaz molekülleri öteleme, dönme ve titreşim hareketi yapar.
- Tanecikleri sürekli hareket halindedir ve kabın iç yüzeyi ve birbirleri ile çarpışarak basınç oluştururlar.
- Bulundukları kabın her yerine yayılarak homojen karışımlar oluştururlar. Kabın yer yerinde basınç aynıdır.
Gazları Tanımlayan Özellikler
Gazların davranışları; sıcaklık, basınç, hacim ve madde miktarı gibi çeşitli değişkenlere bağlı olarak değişebilir.
Basınç
Atmosfer Basıncı: Bir gaz karışımı olan atmosferin yeryüzüne uyguladığı basınçtır. Yükseğe çıkıldıkça azalır. Barometre ile ölçülür.
Gaz Basıncı: Kapalı kapta bulunan gaz taneciklerinin hem birbirleriyle hem de kabın çeperleriyle yaptıkları çarpışmalar sonucunda oluşan kuvvettir. Manometre ile ölçülür.
- Gazların basıncı P ile gösterilir.
- En çok kullanılan basınç birimleri atmosfer (atm) ve mmHg dir.
\(1atm=76cmHg=760mmHg\)
- Birim hacimdeki taneciğin sayısı arttıkça gaz basıncı artar.
- Gaz taneciklerinin hızı ve çarpışma sayısı arttıkça gaz basıncı artar.
Hacim
- Maddelerin boşlukta kapladığı yerdir.
- Bulundukları kabın hacmi, gazların hacmine eşittir.
- Gazların hacmi V (volume) ile gösterilir.
- Gazlarda en çok kullanılan hacim birimi litredir (L).
\(1L=1000mL=1000cm^3\)
Gazların hacmi, sıcaklık ve basınca bağlı olarak değişir.
Bütün gazların 1 molü;
- Standart koşullarda (oda koşulları): (1 atm basınç, 25 santigrat derecede) 24.5L hacim kaplar.
- Normal koşullarda: (1 atm basınç, 0 derecede) 22,4L hacim kaplar.
Sıcaklık
- Sıcaklık, bir maddenin taneciklerinin sahip olduğu kinetik enerjinin ölçüsüdür.
- En çok kullanılan sıcaklık birimleri Kelvin (K, mutlak sıcaklık) ve Celcius* tur.
- Kelvin sıcaklığı T ilei celcius sıcaklığı ise t ile gösterilir.
- Sıcaklık arttıkça gaz taneciklerinin hızı ve ortalama kinetik enerjisi artar. Kinetik enerji, mutlak sıcaklık (K) ile doğru orantılıdır.
- Aynı sıcaklıktaki tüm gazların ortalama kinetik enerjileri eşittir.
\[\text{Kelvin (K)}=\text{Celcius}+273 \]
Miktar
Atom ve moleküller çok küçük tanecikler olduğundan bu taneciklerin miktarını belirlemek için mol kullanılır. Mol n ile gösterilir.
1 mol \(6,02.10^23\) taneciğe karşılık gelir. Aynı sıcaklık ve basınçta tüm gazların 1 er mollerinde \(6,02.10^23\) tane atom ya da molekül bulunur.
Avagadro Sayısı: \(6,02.10^23\) sayısıdır. 1 mol maddenin tanecik sayısını gösterir.
- \(N, N_0\) veya \(N_A\) ile gösterilir.
Mol Kütlesi: Avagadro sayısı kadar taneciğin kütlesidir.
- \(M_A\) ile gösterilir.
- 1 mol \(C\) atomu \(6,02.10^23\) tane atom içerir ve mol kütlesi 12 gram/mol dür.
- 1 mol \(O_2\)'nin mol kütlesi 32 gram/mol dür.
- 1 mol \(CO_2\)'nin mol kütlesi 44 gram/mol dür.
Normal koşullarda 22,4 litre hacim kaplayan bir gaz 1 mol olduğundan \(6,02.10^23\) tanecik içerir.
Hal Değişim Grafikleri
Saf maddeler ısı aldıklarında ya sıcaklıkları artar ya da sabit sıcaklıkta hal değiştirerek katı halden sıvıya ya da sıvıdan gaz hale geçerler.
Saf maddeler ısı verdiklerinde ya sıcaklıkları azalır ya da sabit sıcaklıkta hal değiştirerek gaz halden sıvı hale ya da sıvı halden katı hale geçerler.
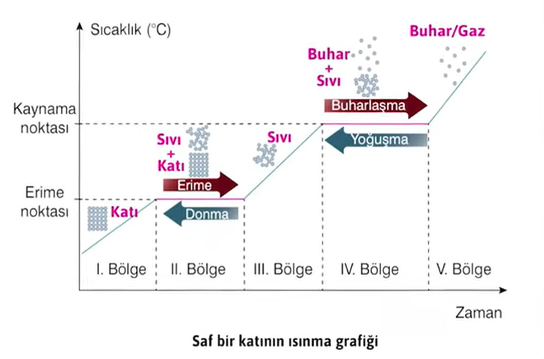
- 1. Bölge: Aldığı ısı etkisi ile sıcaklığı artar. Taneciklerin kinetik enerjisi artar ve titreşim hareketleri hızlanır. Hal değişimi yoktur.
- 2. Bölge: Madde erime sıcaklığındadır ve aldığı ısı sadece erime olayı için kullanılır. Potansiyel enerji artar. Sıcaklık erime süresince sabit kalır. Madde hetorojendir.
- 3. Bölge: Tamamı sıvı hale geçen maddenin aldığı ısı etkisiyle sıcaklık ve kinetik enerjisi artar. Kaynama noktasına gelene kadar madde ayrıca buharlaşır. Madde homojendir.
- 4. Bölge: Madde kaynama sıcaklığındadır ve aldığı ısı sadece buharlaşmada kullanılır. Sıvı tanecikleri arasındaki bağlantı kopup tanecikler bağımsız hale gelir. Sıcaklık kaynama sırasında sabit kalır ve potansiyel enerji artar. Madde heterojendir.
- 5. Bölge: Sıvının tamamı buharlaştıktan sonra sıcaklık tekrar yükselmeye başlar, kinetik enerji de artar. Madde homojendir.
Madde miktarı arttıkça, kaynama süresi de aynı oranda artar. Eğer madde miktarı a iken b süre sonra kaynama oluyorsa, madde miktarı 2a iken 2b süre sonra kaynama olur.
- Yine de maddenin erime/kaynama noktası değişmez.
- Isıtıcının gücü iki katına çıkartıldığında kaynama süresi de iki kat azalır.
Plazma
Gaz haldeki maddeler ısıtılmaya devam edilirse molekülü oluşturan atomlar ve daha sonra da atomlardaki elektronlar kopar.
Plazma: Yüksek sıcaklıklarda molekül, atom, elektron ve katyonlardan oluşan hal. Plazma hali iyonize gaz olarak da tanımlanır.
- Şimşek, yıldırım, mum alevi, kutup ışıkları, volkan lavları plazmaya örnektir.
- Neon lambalarda, gaz yüksek voltaja maruz kaldığı için elektronlar gaz atomlarından ayrılarak daha yüksek enerji seviyesine çıkar. Böylece ampul içindeki gaz plazma haline gelir.
Plazmaların Özellikleri
- Evrendeki en yaygın fiziksel haldir. Evrendeki oranı %99 dan fazladır.
- artı ve eksi yük sayıları eşittir ve elektriksel olarak nötrdürler.
- Elektriği ve ısıyı iyi iletirler.
- Yoğunlukları katı ve sıvılardan küçüktür.
- Birbirleriyle şarpışacak kadar yoğun değildirler.
- Atom, molekül ve iyonlar serbestçe hareket eder.
- Manyetik ve elektriksel alandan etkilenirler.
- Büyük bir enerji yoğunluğuna sahiptirler.
- Plazma halinde tepkimeler daha hızlı gerçekleşir.
Plazmanın Kullanım Alanları
- Neon tabelalar, floresan lambalar ve plazma ekranlar.
- Isıya dayanıklı tıbbi donanım ve sterilizasyon.
- Bakteri öldürücü olarak gıdaların ambalajlanması.
- Dokunun çıkarılması (helyum plazma)
- Kanamayı durdurma (argon plazma)
- Ark kaynakları (as in welding)
Aynı sıcaklıkta gazların kinetik enerjileri eşittir.