TYT-Kimya 16-1. Mol Kavramı-1
- Previous: TYT-Kimya 15-2. Temel Kimya Kanunları-2
- Next: TYT-Kimya 16-2. Mol Kavramı-2
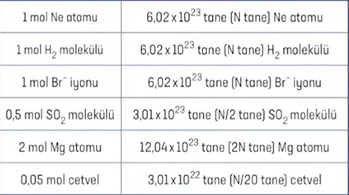
- Avagadro Sayısı: \(6,02x10^{23}\)
- 1 Mol: Avagadro sayısı kadar tanecik.
Mol kavramı, bir maddenin çokluk açısından miktarını ifade etmek için kullanılır. Deste, düzine kavramları gibi sayısal miktarını anlatır.
Avagadro sayısı, \(N\), \(N_A\), \(N_0\) sembolleriyle de gösterilir.
\[mol=\frac{\text{verilen tanecik sayısı}}{\text{avagadro sayısı}} \]
Örnek Sorular

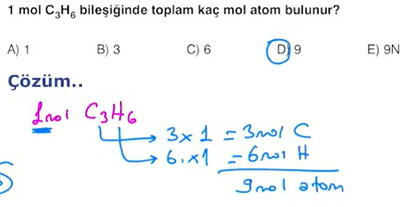
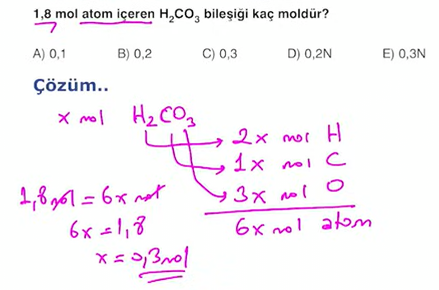

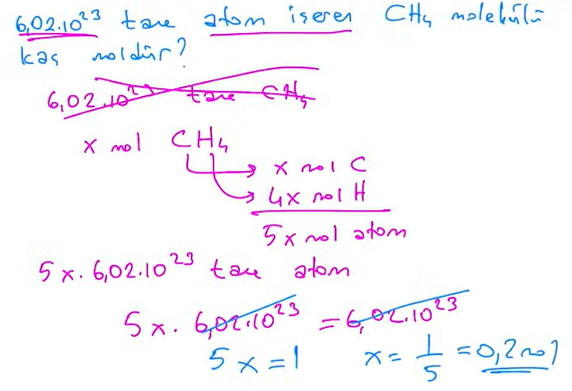
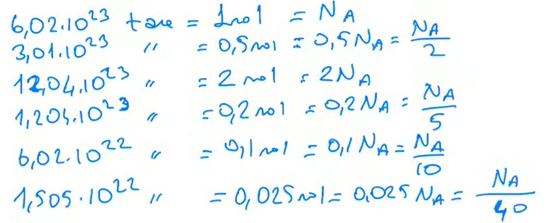
Mol-Hacim İlişkisi
- Gazların birer mollerinin hacimleri aynı koşullarda birbirine eşittir. Buna bağlı olarak aynı şartlarda mol sayıları eşit olan gazların hacimleri eşittir.
- 0 derece celcius ve 1 atm basınç altında (normal koşullar) 1 mol gazın hacmi \(22,4\) litredir.
- 25 derece celcius ve 1 atm basınç altında (oda koşulları/standart koşullar) 1 mol gazın hacmi \(24,5\) litredir.
Normal Şartlarda:
\[\text{Mol Sayısı (n)}=\frac{Hacim (L)}{22,4} \]
Oda Şartlarında
\[\text{Mol Sayısı (n)}=\frac{Hacim (L)}{24,5} \]

Örnek Sorular



