TYT-Kimya 16-2. Mol Kavramı-2
- Previous: TYT-Kimya 16-1. Mol Kavramı-1
- Next: -
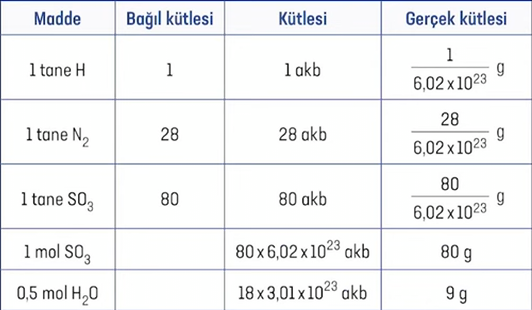
Mol-Kütle Iliskisi
- Mol Kütlesi: 1 mol maddenin, gram cinsinden kütlesine mol kütlesi veya mol ağırlığı denir.
- Birimi: \(g/mol\)
Atomlar, moleküller, iyonlar, proton, nötron vb. tanecikler çok küçük maddelerdir. Bu nedenle bu maddelerin kütlelerini ifade etmek için çok daha küçük bir kütle birimi türetilmiştir
- Bu birim atomik kütle birimidir ve akb ile gösterilir.
-
Atomik Kütle Birimi: \({}^{12}C\) atomunun kütlesinin 12 de biri 1 akb olarak tanımlanır. Buna göre, 1 tane \({}^{12}C\) atomunun kütlesi 12 akb dir.
-
Bağıl Atom Kütlesi: Bir atomun \({}^{12}C\) atomu ile kıyaslanarak bulunan kütlesine denir. Başka bir ifadeyle bağıl atom kütlesi, bir atomun kütlesinin 1 akb nin kaç katı olduğunu gösterir.
O:16 Oksijenin bağıl atom kütlesi 16 dır. 1 tane oksijen atomunun kütlesi 16 akb dir. 1 mol oksijen atomunun kütlesi 16 gramdır.
- 1 gram = \(6,02.10^{23}akb\)
- 1 akb = \(1 gram / 6,02.10^{23}\)
- 1 gram = \(N akb\)
- 1 akb = \((1/N)gram\)
- \(1mol.1akb \text{(mol kütlesi)} = 1 gram\)
\[X akb = \frac{X}{N} gram \]
\[X gram = X.N akb \]
- X: verilen maddenin birim kütlesi (bağıl atom kütlesi)
\[n\text{(Mol Sayısı)}=\frac{\text{Kütle}(gram)}{M_A\text{(akb)}} \]
\(mol=gram/akb\)
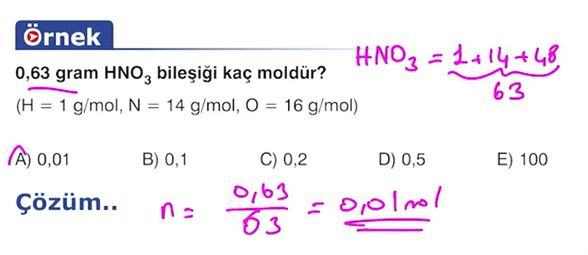

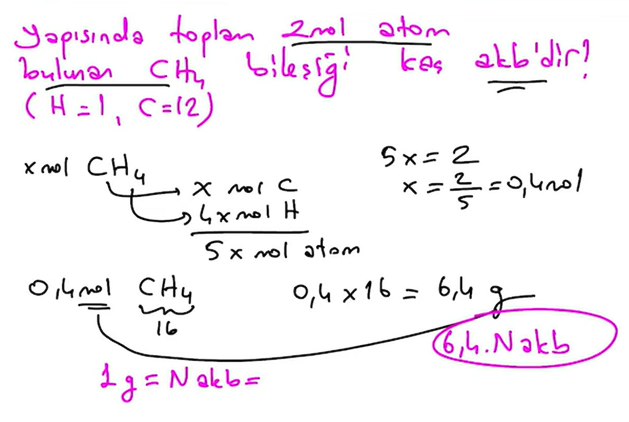
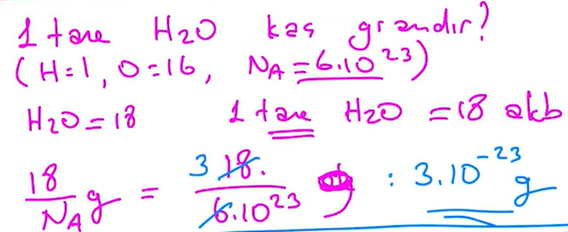
Aşağıdaki kavramların tamamı mol anlamına gelir. Bu kavramlar uygun maddeler için kullanılır.
- Atom-gram: Atomik yapıdaki maddeler için kullanılır.
- Molekül-gram: kovalent bağlı moleküller için kullanılır.
- Formül-gram: iyonik bağlı bileşikler için kullanılır.
- İyon-gram: iyonlar için kullanılır.


Karışımlarda Mol Hesabı


İzotop Atomlar ve Ortalama Atom Kütlesi
Bir elementin tüm atomlarında proton sayısı aynıdır. Ancak aynı elementin farklı atomlarında farklı sayılarda nötron bulunabilir. Bu tür atomlar birbirinin izotopudur. İzotop atomların atom ağırlıkları birbirinden farklıdır. Bir element tabiatta izotoplarının karışımı halinde bulunduğundan atom ağırlığı bu durum dikkate alınarak hesaplanır.
- Ortalama Atom Kütlesi: Bir elementin atom kütlesinin, izotop atomlarının tabiatta bulunma oranları dikkate alınarak hesaplanan ağırlıklı ortalamasıdır.
\[OAK=\frac{\text{1.iy x 1.iak}}{100}+\frac{\text{2.iy x 2.iak}}{100}+\text{...} \]
- oak: ortalama atom kütlesi
- iy: izotop yüzdesi
- iak: izotopun atom kütlesi
